EUDAMED obrigatória a partir de 28 de maio de 2026

A EUDAMED IRÁ FINALMENTE SER OBRIGATÓRIA A PARTIR DE 28 DE MAIO DE 2026!
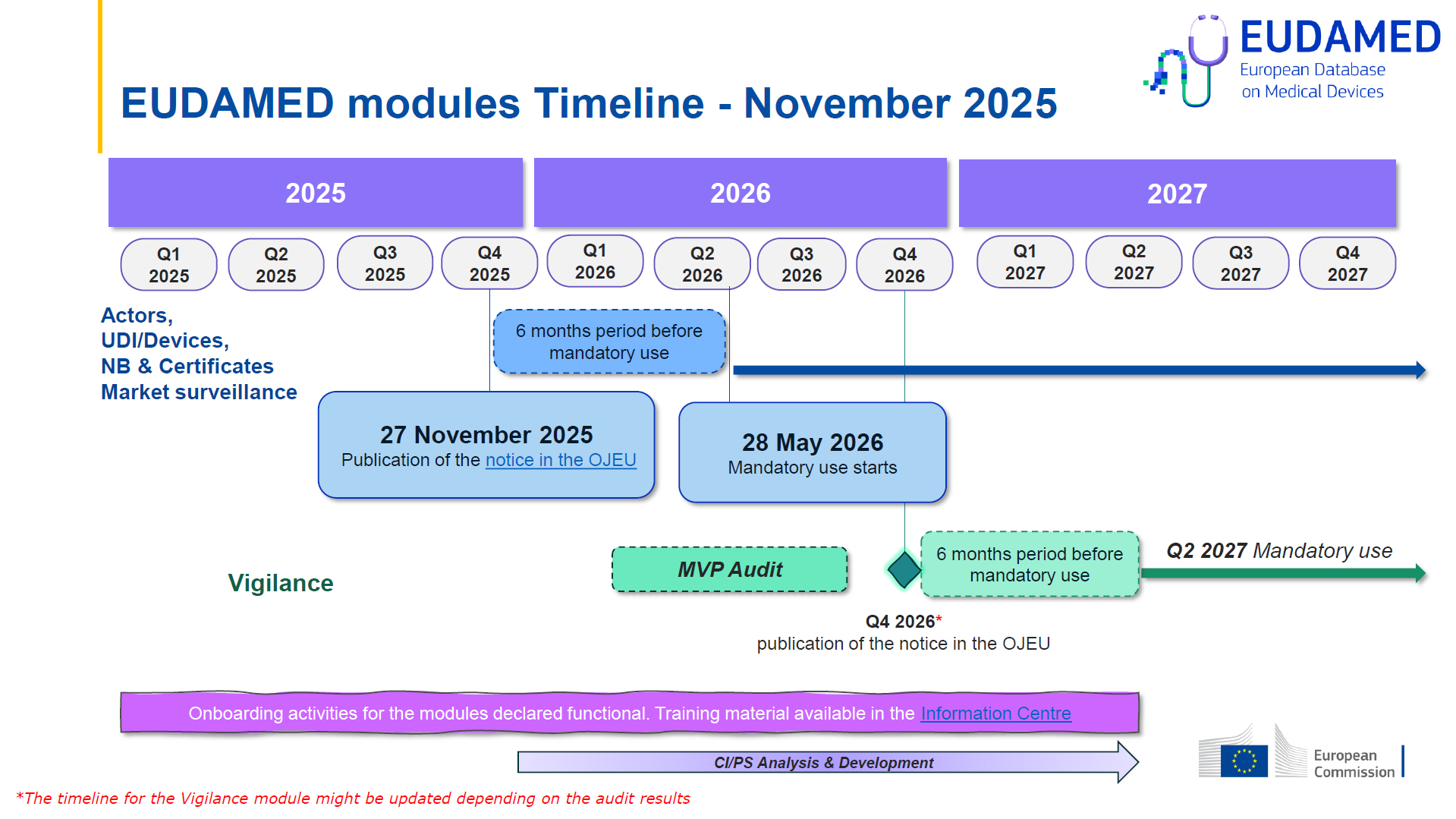
O aviso oficial foi publicado pela Comissão Europeia no Jornal Oficial da União Europeia a 27 de novembro de 2025, iniciando o período de transição de seis meses, que termina em 28 de maio de 2026.
A partir desta data, os primeiros quatro módulos da EUDAMED serão obrigatórios, representando um passo decisivo para fabricantes, mandatários, importadores e organismos notificados na União Europeia.
QUAIS OS MÓDULOS QUE SE TORNAM OBRIGATÓRIOS
A partir de 28 de maio de 2026, os seguintes módulos passam a ser de uso obrigatório:
- Actor Registration – registo de operadores económicos (fabricantes, mandatários, importadores, etc.)
- UDI/Devices Registration – registo de dispositivos e UDI
- Notified Bodies & Certificates – registo de organismos notificados e certificados
- Market Surveillance – módulo de suporte à fiscalização e monitorização do mercado, que facilita a coordenação entre as Autoridades Competentes
DATAS PRINCIPAIS A TER EM CONTA
| MARCO | DATA |
| Publicação do aviso no OJEU | 27 Novembro 2025 |
| EUDAMED obrigatória (4 módulos) | 28 Maio 2026 |
| Aviso relativo ao Módulo de Vigilância no OJEU | Q4 2026 |
| Módulo de Vigilância obrigatório | Q2 2027 |
O QUE MUDA E PORQUE É RELEVANTE
- O registo de operadores económicos passa a ser obrigatório antes de colocar dispositivos no mercado; sem registo, não é possível usar os outros módulos.
- O registo de novos dispositivos médicos/UDI torna-se estratégico para a colocação do produto no mercado
- Os Organimos notificados devem registar novos certificados na EUDAMED partir de 28/05/2026 e certificados existentes até 27/05/2027.
- As Autoridades Competentes dos Estados-Membros têm na EUDAMED uma ferramenta harmonizada para fiscalização e coordenação do mercado.
A obrigatoriedade destes módulos representa um grande passo para a transparência, segurança e rastreabilidade dos dispositivos médicos na União Europeia. A preparação antecipada é essencial para evitar atrasos, sobrecarga de registos e problemas de conformidade!
COMO A ALL4COMPLIANCE PODE AJUDAR
A All4Compliance apoia fabricantes, mandatários e importadores a garantir que a sua empresa e os seus produtos cumpram totalmente os novos prazos da EUDAMED. Podemos ajudá-lo a planear e gerir todo o processo, desde a avaliação de prontidão e estratégia de registo, à preparação e submissão de dados de dispositivos, passando por consultoria regulatória e formação sobre a EUDAMED.
O nosso objetivo é tornar a implementação da EUDAMED o mais simples e eficiente possível, reduzindo riscos de erros, atrasos e problemas de conformidade associados.
Entre em contacto connosco para garantir uma proposta adaptada às necessidades da sua empresa, dos seus produtos, e garantir que cumpre os novos prazos obrigatórios!


Morada
Biocant Park | Núcleo 04 Lote 2 |
3060-197 Cantanhede
Portugal
Redes Sociais
© All4Compliance. Todos os direitos reservados. Desenvolvido por Bestsites.pt